Triangolo di Van Arkel-Ketelaar


Il Triangolo di Van Arkel-Ketelaar (dal nome degli scienziati Anton Eduard van Arkel e J. A. A. Ketelaar) è una pratica rappresentazione grafica, utilizzata in chimica, per individuare il "carattere" del legame che si forma tra due elementi chimici: ionico, covalente o metallico (è un metodo alternativo per la classificazione dei legami).
Il triangolo di Van Arkel-Ketelaar riporta sull'asse y la differenza di elettronegatività tra i due elementi considerati e sull'asse x l'elettronegatività media degli elementi nel composto.
Nella regione in basso a sinistra del triangolo vengono a posizionarsi le specie più metalliche, ossia con differenza di elettronegatività nulla(zero sull'asse y) in quanto si tratta di composti formati da atomi uguali (e quindi con pari elettronegatività) e elettronegatività media degli elementi bassa essendo essi elementi metallici, quindi dotati tipicamente di bassa o medio-bassa elettronegatività. Il composto più metallico in assoluto, ossia esattamente al vertice del triangolo è il Cesio (Cesio metallico zerovalente, a rigore sarebbe il Francio metallico, ma è instabile).
Nella regione in basso a destra del triangolo vengono a posizionarsi le specie più covalenti, ossia con differenza di elettronegatività nulla(sono specie formate da atomi uguali) ed elettronegatività media degli elementi alta essendo tipicamente non metalli ad elevata elettronegatività. Il composto più covalente in assoluto, ossia esattamente al vertice in basso a destra del triangolo è F2 (gas Fluoro).
Nella regione in alto al centro del triangolo vanno a posizionarsi le specie più ioniche, ossia con differenza di elettronegatività massima, essendo formate da un composto molto elettronegativo ed uno poco elettronegativo ed elettronegatività media di valore intermedio. Il composto più ionico è rappresentato come si può dedurre da quanto detto sopra dal CsF (Floruro di Cesio).
Nelle regioni centrali vanno quindi a posizionarsi tutte le specie con valori intermedi.
-
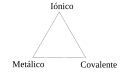 Triangolo di ketelaar
Triangolo di ketelaar
Altri progetti
Altri progetti
- Wikimedia Commons
 Wikimedia Commons contiene immagini o altri file su Triangolo di Van Arkel-Ketelaar
Wikimedia Commons contiene immagini o altri file su Triangolo di Van Arkel-Ketelaar
 Portale Chimica
Portale Chimica Portale Fisica
Portale Fisica











